|
|||||||
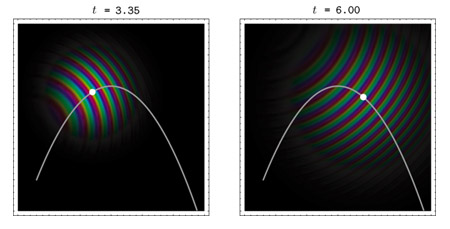
Die Farben der WellenfunktionWie wir gesehen haben, beschreibt die Quantenmechanik so einen alltäglichen Vorgang, wie die Bewegung eines Teilchens durch den Raum, als Ausbreitung einer Wellenfunktion. Die so beschriebenen Elektronen haben einerseits Teilchennatur (sie werden an bestimmten Orten mit gewissen Wahrscheinlichkeiten gefunden), aber auch Wellennatur, die, wie schon der Name sagt, von der Wellenfunktion beschrieben wird. Die Farben in den Bildern beschreiben diese Wellennatur etwas genauer. Der Abstand der gleichfarbigen Streifen deutet die durchschnittliche Wellenlänge an diesem Ort an. Es gibt nun einen fundamentalen Zusammenhang: Kurze Wellenlänge = Hohe Geschwindigkeit (daher hohe kinetische Energie) Lange Wellenlänge = Langsame Geschwindigkeit (daher niedrige kinetische Energie)
Die Linien gleicher Farbe sind so etwas wie die Wellenkämme und Wellentäler. Diese sind immer senkrecht auf die Ausbreitungsrichtung der Wellenfunktion. Die Farben deuten aber an, daß man sich die Wellenfunktion nicht wie eine Wasserwelle oder eine Druckwelle vorstellen soll. Die quantenmechanische Wellenamplitude ist eine zweidimensionale Größe: mathematisch wird sie durch eine sogenannte "komplexe Zahl" beschrieben. Warum sind Gammastrahlen gefährlich?Der Zusammenhang zwischen Wellenlänge und Energie ist für uns von großer Bedeutung. Auch das Licht besteht nämlich aus Teilchen ("Photonen"), die gleichzeitig als Welle in Erscheinung treten können ("Lichtwelle"). Photonen fliegen zwar immer mit Lichtgeschwindigkeit (300000 km/sec), aber ihr Impuls und damit die kinetische Energie hängen genauso von der Wellenlänge ab, wie bei quantenmechanischen Tennisbällen (Elektronen). Bei vergleichsweise langwelliger Strahlung (Radiowellen, Infrarotstrahlung, sichtbares Licht) ist die Energie der Photonen nur gering, und die Strahlung ist für uns harmlos. Hochenergetische Photonen sind aber gefährlich, weil sie unsere Zellen beschädigen können. Solche Photonen mit hoher kinetischer Energie tauchen in kurzwelliger elektromagnetischer Strahlung auf:
Je kürzer die Wellenlänge, desto höher die Energie der Photonen, und desto höher ist das Verletzungsrisiko, wenn wir uns dieser Strahlung aussetzen. Im Prinzip ist jedes einzelne kurzwellige Photon bereits gefährlich, aber natürlich hängt das Verletzungsrisiko von der Anzahl der Photonen, also von der Intensität der Strahlung ab. |
|||||||
7 |
|||||||
| Author: Bernd Thaller Created: Dec 15 2000. Last modified: Dec 15, 2000 |
|||||||